L'équilibrage des équations chimiques
Comment conciliez-vous une équation chimique?
Dans une masse de réaction chimique est toujours conservée. Cela signifie que la matière ne soit pas créée ni détruite.
Vous ne pouvez pas transformer des atomes de plomb en atomes d'or dans une réaction chimique!
Dans une réaction, les mêmes atomes sont simplement réarrangées que les anciens liaisons chimiques sont brisées et de nouvelles liaisons sont formées.
Les produits chimiques qui réagissent sont appelés les réactifs. Les nouveaux produits chimiques qui sont produites sont appelés les produits.
Les équations chimiques sont équilibrées en plaçant des nombres entiers devant les formules chimiques.
Une équation est équilibré lorsque le nombre et le type d'atomes réactif est le même que le nombre et le type d'atomes de ce produit.
Remarque: Vous ne changez pas la formule chimique d'une substance pour équilibrer une équation chimique.
Exemples d'équations chimiques équilibrées
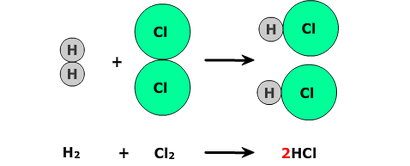
Une molécule d'hydrogène réagit avec une molécule de chlore pour produire deux molécules de chlorure d'hydrogène.
Les nombres entiers sont placés en face de la formule chimique (en rouge) pour équilibrer une équation.
Comme en algèbre un 1 n'est pas nécessaire si H2 est écrit au lieu de 1H2 et Cl2 est écrit au lieu de 1Cl2
Vérifions si les atomes sont équilibrés.